Григорьянц А.А.
ОСОБЕННОСТИ ПЕРЕМЕЩЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ И ФАРМАЦЕВТИЧЕСКИХ СУБСТАНЦИЙ
УДК 339.545
А.А. Григорьянц, студент факультета таможенного дела Ростовского филиала Российской таможенной академии
e-mail: anastasiagrigoryants@gmail.com
Аннотация. В статье раскрываются основные аспекты организационно-правового регулирования перемещения лекарственных средств и фармацевтических субстанций через таможенную границу. Автором определены основные особенности совершения таможенных операций в отношении лекарственных средств и фармацевтических субстанций. Авторские выводы основываются на изучении практических аспектов совершения таможенных операций с лекарственными средствами и фармацевтическими субстанциями.
Ключевые слова: запреты и ограничения, лекарственные средства, фармацевтические субстанции, нетарифное регулирование внешнеэкономической деятельности, таможенный контроль, разрешительный порядок.
Введение
В настоящее время в условиях пандемии новой коронавирусной инфекции и экономических санкций, введенных в отношении Российской Федерации, создаются определенные проблемы с ввозом в страну такой важной категории товаров как лекарственные препараты. Многие лекарственные средства, в том числе и те, которые помогают облегчить состояние при орфанных и тяжелых заболеваниях, производятся только в европейских странах или США. В связи с нынешней геополитической обстановкой одни импортеры ищут способы ввоза в страну привычных лекарственных средств при помощи параллельного импорта, другие пытаются ввозить фальсифицированные и некачественные лекарственные средства и фармсубстанции, что может повлиять на здоровье людей или даже создать угрозы их жизни.
Принимая во внимание данную ситуацию, государство создает механизмы, позволяющие помочь импортерам при совершении таможенных операций в отношении качественных и эффективных лекарственных средств и фармсубстаций, но препятствующие попытки перемещения фальсифицированных товаров, отражая все актуальные изменения в законодательстве как на национальном, так и наднациональном уровнях.
Цель статьи – проанализировать отличительные особенности совершения таможенных операций и проведения таможенного контроля в отношении лекарственных средств и фармацевтических субстанций, перемещаемых через таможенную границу ЕАЭС.
Лекарственные средства и фармсубстанции как отдельная категория товаров.
Изначально стоит отметить тот факт, что вопросы регулирования перемещения лекарственных препаратов и фармсубстанций поделены между национальным и наднациональным уровнями (рис. 1). Страны-участницы ЕАЭС поэтапно гармонизируют законодательство и механизмы регулирования и функционирования общего рынка, но такие аспекты как экономические и культурные различия делают унификацию внутреннего рынка ЕАЭС невозможной.

Рис. 1. Особенности регулирования обращения лекарственных средств в рамках ЕАЭС
В связи с таким разделением организационно-правовые основы перемещения лекарственных средств и фармацевтических субстанций прописаны в Решении Коллегии ЕЭК от 21.04.2015 № 30 «О мерах нетарифного регулирования» (далее — Решение Коллегии ЕЭК № 30) [1], то есть это единые правила, которых придерживаются все страны-участницы, но национальное законодательство их может уточнять. В Российской Федерации такими уточняющими правовыми актами являются Федеральный закон «Об обращении лекарственных средств» [2] и Постановление Правительства РФ от 01.06.2021 № 853 [3].
Если обратиться к ст. 4 Федерального закона «Об обращении лекарственных средств», то можно найти определение лекарственных средств как веществ либо их комбинаций, вступающих в контакт с организмом и проникающих в его органы и ткани, которые применяются для:
а) профилактики, диагностики и лечения заболевания;
б) реабилитации;
в) сохранения, предотвращения или прерывания беременности.
Они включают в себя фармацевтические субстанции и лекарственные препараты. Последние представляют собой средства в лекарственных формах, а фармацевтическая субстанция обычно выступает в качестве одного или нескольких действующих веществ вне зависимости от природы происхождения, которые обладают фармакологической активностью и предназначены для изготовления лекарственных препаратов.
Лекарственные средства во всем разнообразии их форм, особенностей и силы воздействия являются особой категорией товаров в силу возможности их влияния на организм человека. Отдельные субстанции или фальсифицированные лекарственные средства в целях извлечения прибыли могут навредить отдельным лицам в силу таких особенностей при взаимодействии с человеческим организмом. Исходя из этого, их производство, реализация, а также перемещение находятся в зоне внимания, как субъектов фармацевтического рынка, так и контролирующих органов.
Разрешительный порядок ввоза лекарственных средств и фармацевтических субстанций
Лекарственные средства при перемещении через таможенную границу Евразийского экономического союза подпадают под меры нетарифного регулирования. Лекарственные средства и фармацевтические субстанции входят в Единый перечень (а именно раздел 2.12), утвержденный Решением Коллегии ЕЭК № 30.
Примечателен тот факт, что в зависимости от состава лекарственные средства могут относиться к разным разделам Единого перечня. Если в состав препарата входят наркотические или психотропные вещества либо из прекурсоры, то они относятся к разделу 2.12. «Наркотические средства, психотропные вещества и их прекурсоры», и будут ввозиться по лицензии, которые выдает уполномоченный орган — Министерство промышленности и торговли. Лекарственные средства и фармсубстанции без таких веществ относятся к разделу 2.14. «Лекарственные средства» и перемещаются по заключению (разрешительному документу), выдаваемому Министерством Здравоохранения (рис. 2).

Рис. 2. Отнесение лекарственных средств и фармацевтических субстанций к разделам Единого перечня
Участники ВЭД могут ввозить только зарегистрированные лекарственные средства, внесенные в государственный реестр лекарственных средств (ГРЛС) (рис. 3), кроме случаев, когда физические лица ввозят их для личного использования или потребления; лекарственные средства ввозятся пассажирами или членами экипажей транспортных средств; предназначены для лечения участников различных культурных и спортивных мероприятий и экспедиций. Также незарегистрированные лекарственные препараты могут ввозиться с целью их экспертизы и дальнейшей регистрации с внесением в ГРЛС.
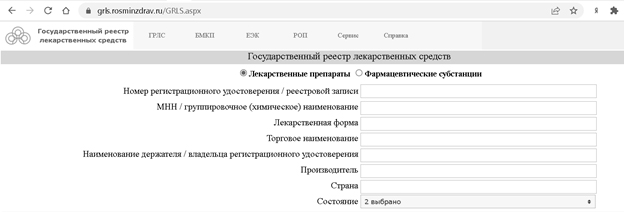
Рис. 3. Страница поиска по ГРЛС на официальном сайте Минздрава
Стоит отметить ещё тот факт, что при помещении лекарственных препаратов и фармсубстанций под такие таможенные процедуры как переработка на таможенной территории, таможенный склад, свободная таможенная зона, свободный склад, уничтожение, таможенный транзит, а также зарегистрированных лекарственных средств под таможенную процедуру временного ввоза представление заключения Минздрава таможенному органу можно не предоставлять. Также лекарственные средства не могут быть реализованные в магазинах беспошлинной торговли, так как не допускается их помещение под таможенную процедуру беспошлинной торговли.
Практические аспекты совершения таможенных операций с лекарственными средствами и фармсубстанциями
Для обеспечения законности совершения таможенных операций с лекарственными препаратами и фармацевтических субстанциями таможенными органами применяется такая форма таможенного контроля как проверка таможенных документов и сведений. Декларант при подаче декларации в таможенный орган указывает заключение Минздрава разрешительный документ, позволяющий ему осуществлять внешнеторговые операции с лекарственными средствами (код документа в 44 графе ДТ – 01081). Также в данной графе должна быть указана лицензия на осуществление фармацевтической или медицинской деятельности в зависимости от предприятия, которое ввозит лекарственные средства и фармсубстанции.
Лекарственные препараты входят в перечень товаров, подлежащих обязательной маркировке. Это необходимо для контроля за их оборотом на территории РФ и, при необходимости, изъятия недоброкачественных, фальсифицированных или же контрафактных лекарственных средств и фармсубстанций. Данная мера предполагает нанесение специальных контрольных идентификационных знаков (КИЗ) на упаковку товара перед вводом в оборот (рис. 4).

Рис. 4. Контрольный идентификационный знак на упаковке лекарственного препарата
Для нанесения маркировки при импорте партии лекарственных средств необходимо поместить её под таможенную процедуру таможенного склада. Выбранный таможенный склад должен иметь лицензию на осуществление фармацевтической деятельности. Процесс нанесения маркировки должен осуществляться в зоне таможенного контроля. Сами КИЗ должны быть заблаговременно запрошены в системе Мониторинга движения лекарственных средств, оплачены и зарегистрированы [4]. Далее полученные от системы маркировки наносятся на упаковку на каждую единицу товара. Потом на каждом этапе оборота лекарственных средств маркировка сканируется, и в системе делается соответствующая отметка. Таким образом можно проследить весь путь товара от производителя к конченому покупателю и выяснить, был ли он введен в оборот незаконно. Отсутствие маркировки на упаковке также будет говорить о незаконности ввода в оборот.
Таблица 1
Перечень таможенных складов
| Владелец таможенного склада | Таможенный орган |
| АО «Норстон» (Сантенз) | Московская областная таможня |
| ООО «Объединенная таможенно-логистическая компания» | Московская областная таможня |
| АО «ОРФЕ» | Московская областная таможня |
| ЗАО «АЙТЕМС СКЛАДЫ» | Московская областная таможня |
| ООО «ТС ТРАНССЕРВИС» | Московская областная таможня |
| ООО «АСФАРМА-РОС» | Татарстанская таможня |
| ПАО «Биосинтез» | Саратовская таможня |
Все таможенные склады с лицензией на осуществление фармацевтической деятельности расположены в европейской части РФ в Центральном и Приволжском федеральных округах, так как основной поток лекарственных средств идет из стран Европейского Союза и США (табл. 1). К сожалению, данный факт является проблемой, так как в связи с введенными в отношении РФ экономическими санкциями основной поток товаров идет из азиатских стран, которые находятся на большом расстоянии от данных таможенных складов.
Выводы Таким образом, лекарственные препараты представляют собой важную категорию товаров как для национальных интересов Российской Федерации в области здравоохранения, так и для таможенного регулирования. Тщательный и всесторонний контроль за перемещением данной категории товаров обусловлен тем, что лекарственные средства представляют важность для обеспечения здоровья населения страны, но ввоз недоброкачественных или фальсифицированных лекарственных препаратов и фармсубстанций может легко его подорвать. Порядок ввоза лекарственных средств и фармацевтических субстанций закреплен, в первую очередь, на уровне права ЕАЭС. Эта продукция входит в Единый перечень товаров, в отношении которых применяются меры нетарифного регулирования при их перемещении через таможенную границу ЕАЭС. Вместе с тем проверка обеспечения соблюдения запретов и ограничений осуществляется только при их ввозе. Перед государством в нынешних условиях стоит задача максимально, на сколько это возможно, облегчить условия ввоза лекарственных средств для обеспечения нужд населения, но не потерять при этом качество контроля за недоброкачественными и фальсифицированными препаратами.
Использованные источники:
- Решение Коллегии Евразийской экономической комиссии от 21.04.2015 № 30 «О мерах нетарифного регулирования». [Электронный ресурс] // Официальный интернет-портал правовой информации. URL: http://www.pravo.gov.ru
- Федеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств». [Электронный ресурс] // Официальный интернет-портал правовой информации. URL: http://www.pravo.gov.ru
- Постановление Правительства РФ от 01.06.2021 № 853 «Об утверждении Правил ввоза лекарственных средств для медицинского применения в Российскую Федерацию и признании утратившими силу некоторых актов и отдельных положений некоторых актов Правительства Российской Федерации». [Электронный ресурс] // Официальный интернет-портал правовой информации. URL: http://www.pravo.gov.ru
- Информация Росздравнадзора от 01.03.2021 «Описание процесса маркировки лекарственных препаратов на таможенном складе». [Электронный ресурс] // Официальный интернет-портал правовой информации. URL: http://www.pravo.gov.ru
- Информация ФТС о ввозе и пересылке лекарственных средств [Электронный ресурс] // Официальный сайт ФТС России. URL: https://customs.gov.ru/fiz/pravila-peremeshheniya-tovarov/lekarstvennye-sredstva
